Além da bolsa: um guia abrangente para o conjunto de transfusão de sangue
Jul 22,2025
I. Introdução aos conjuntos de transfusão de sangue
UM transfusão sanguínea é um procedimento médico que salva vidas que envolve transferir componentes sanguíneos ou sanguíneos de um doadou para a courente sanguínea de um destinatário.
UM jornada da transfusão de sangue e, consequentemente, a evolução dos dispositivos usados para ela, abrange séculos.
Na medicina moderna, o conjunto de transfusão de sangue é uma ferramenta indispensável, desempenhando um papel vital em uma vasta gama de cenários clínicos.
Ii. Componentes de um conjunto de transfusão de sangue padrão
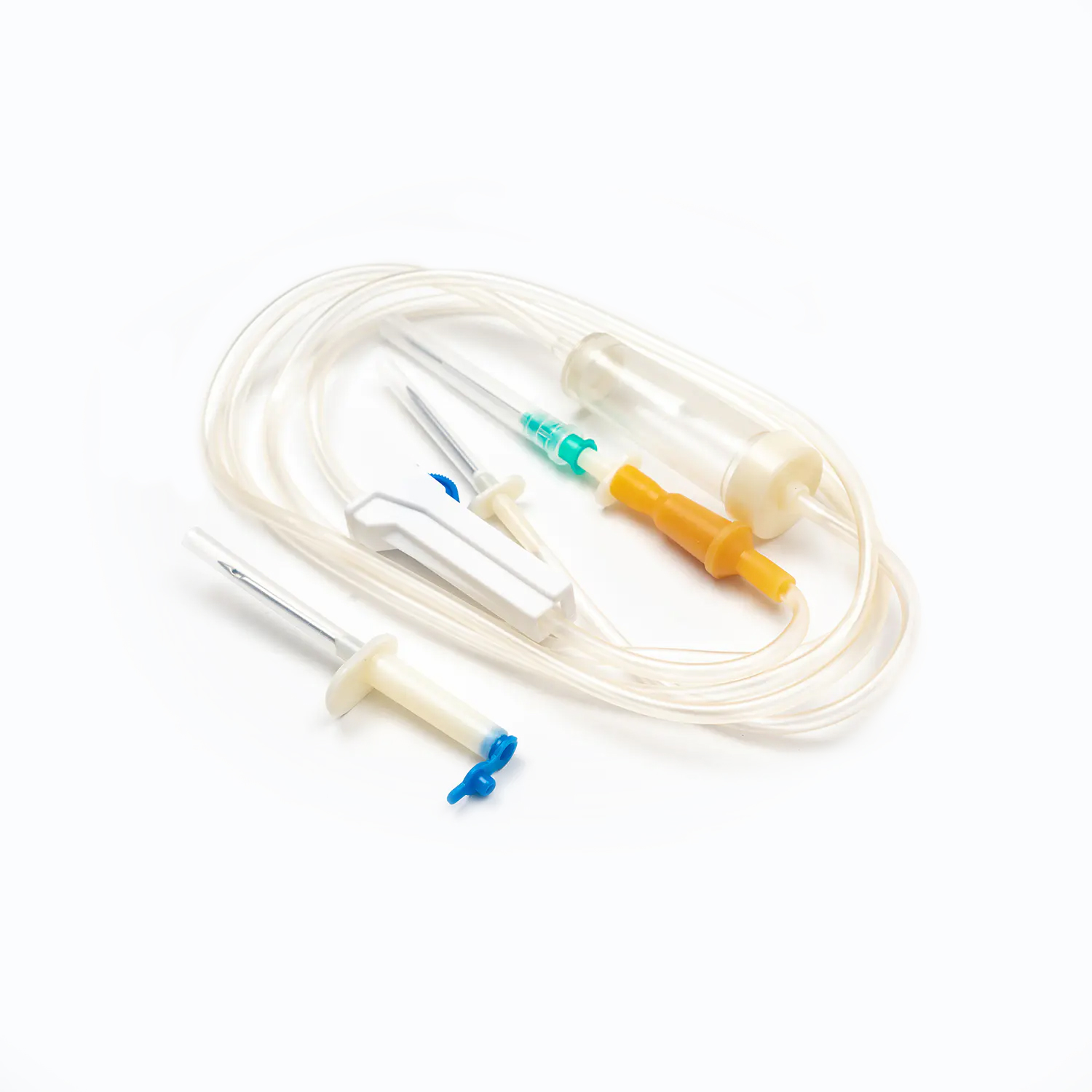
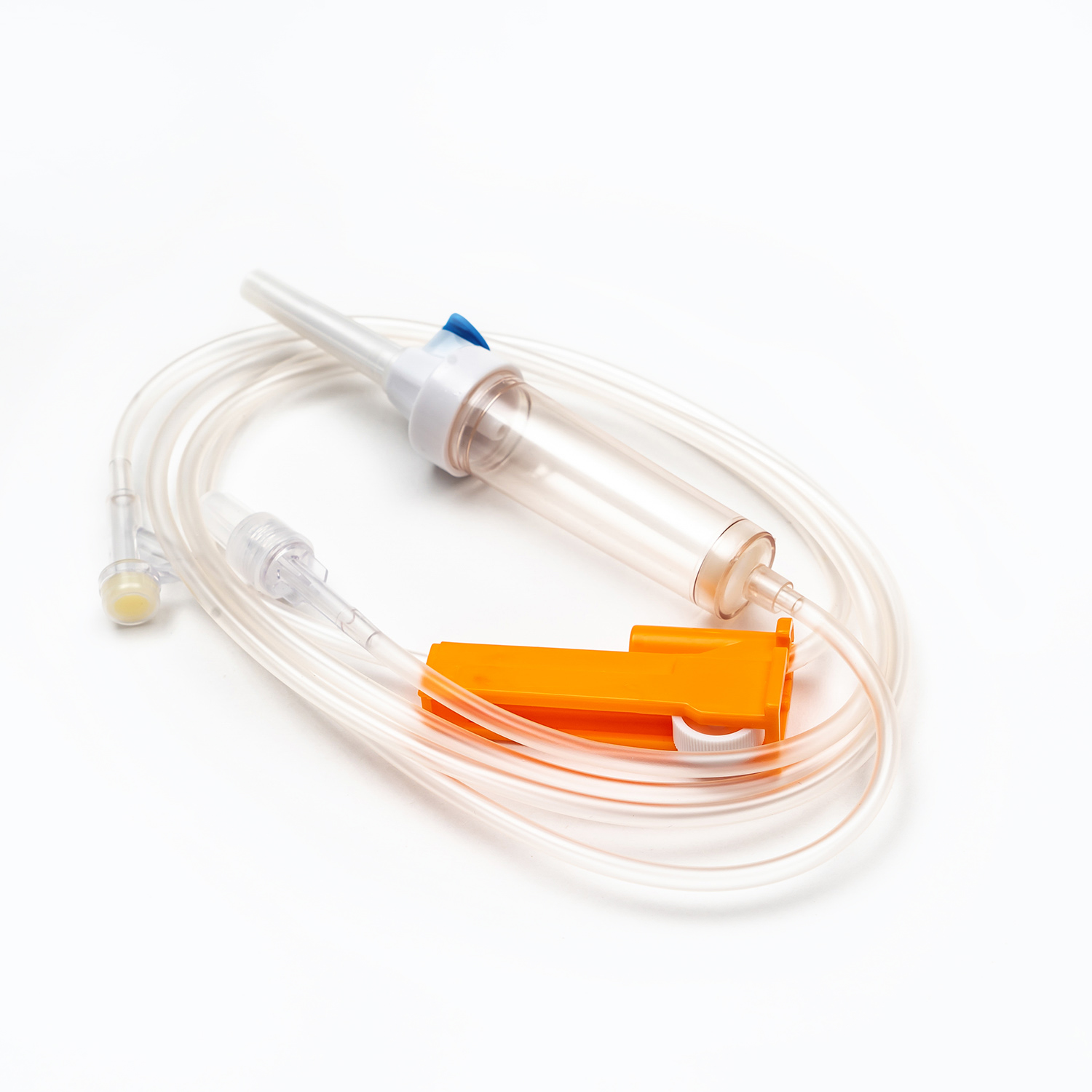
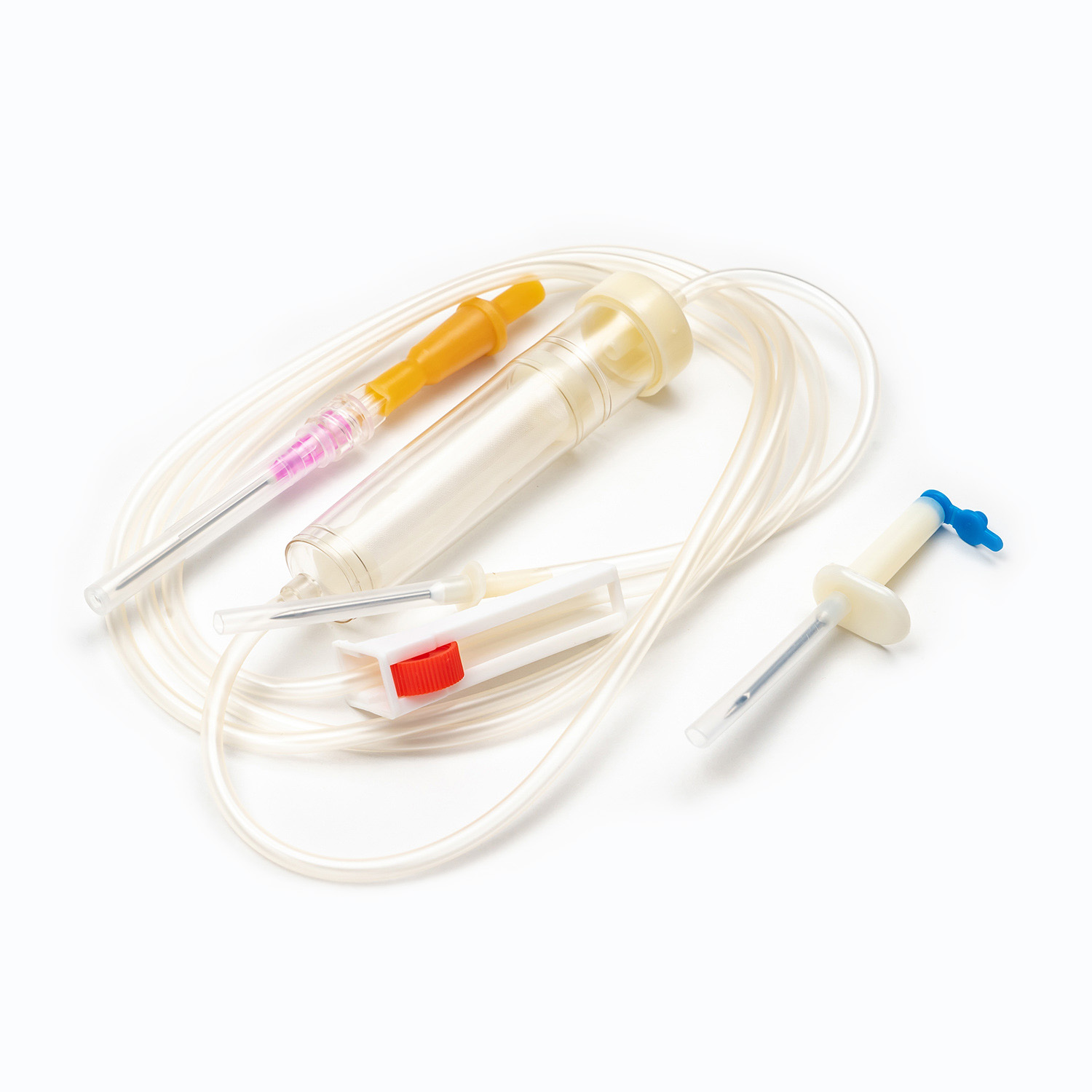
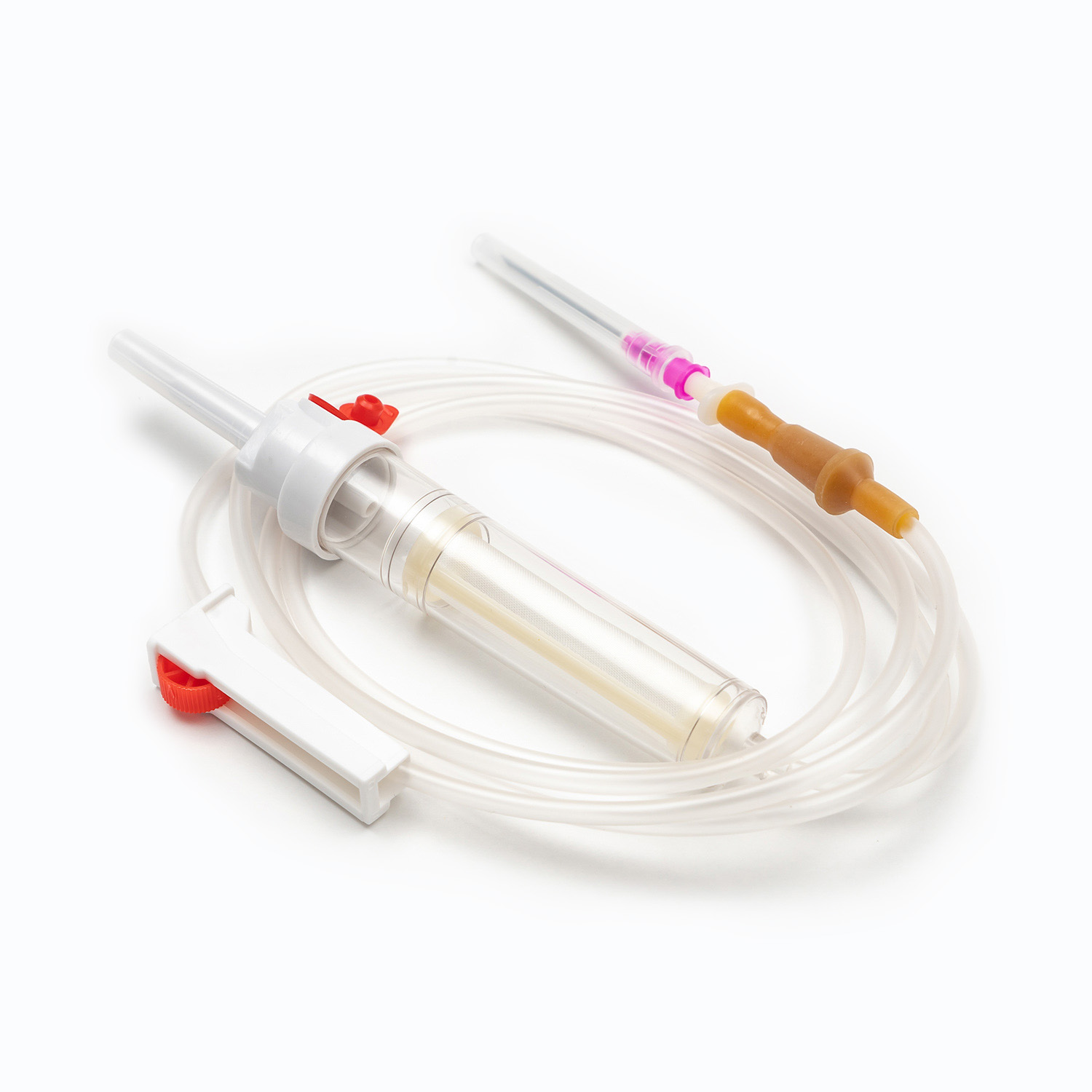
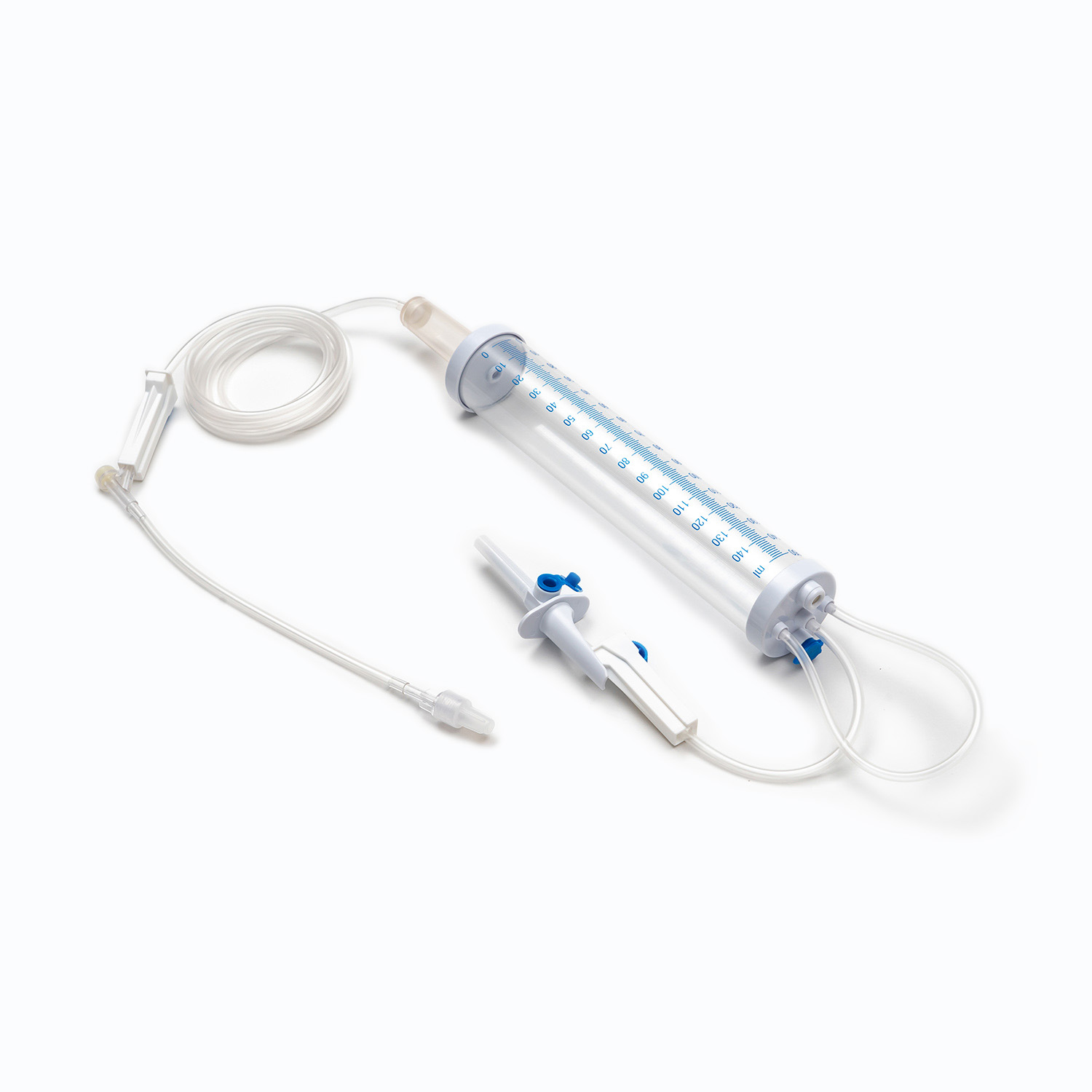
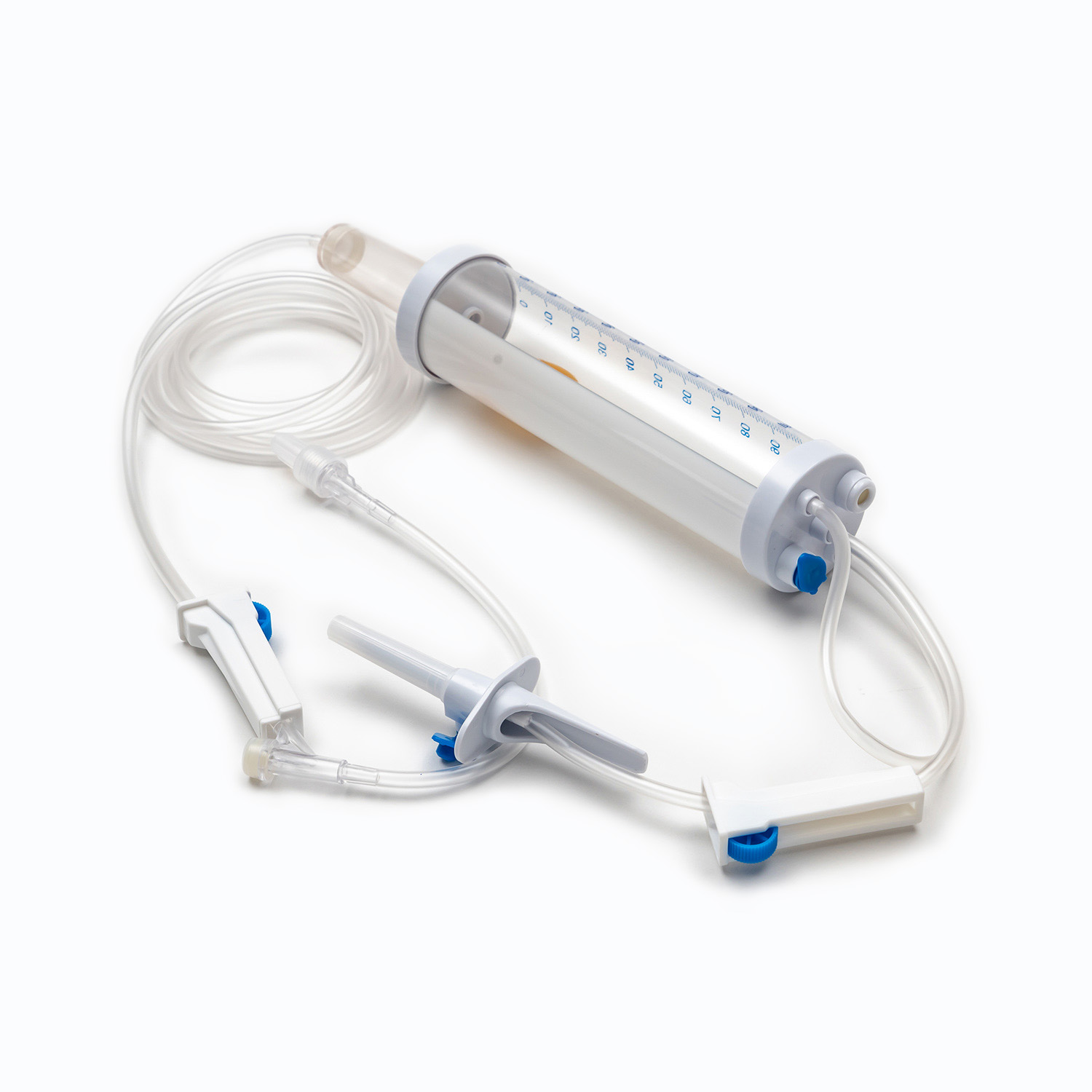
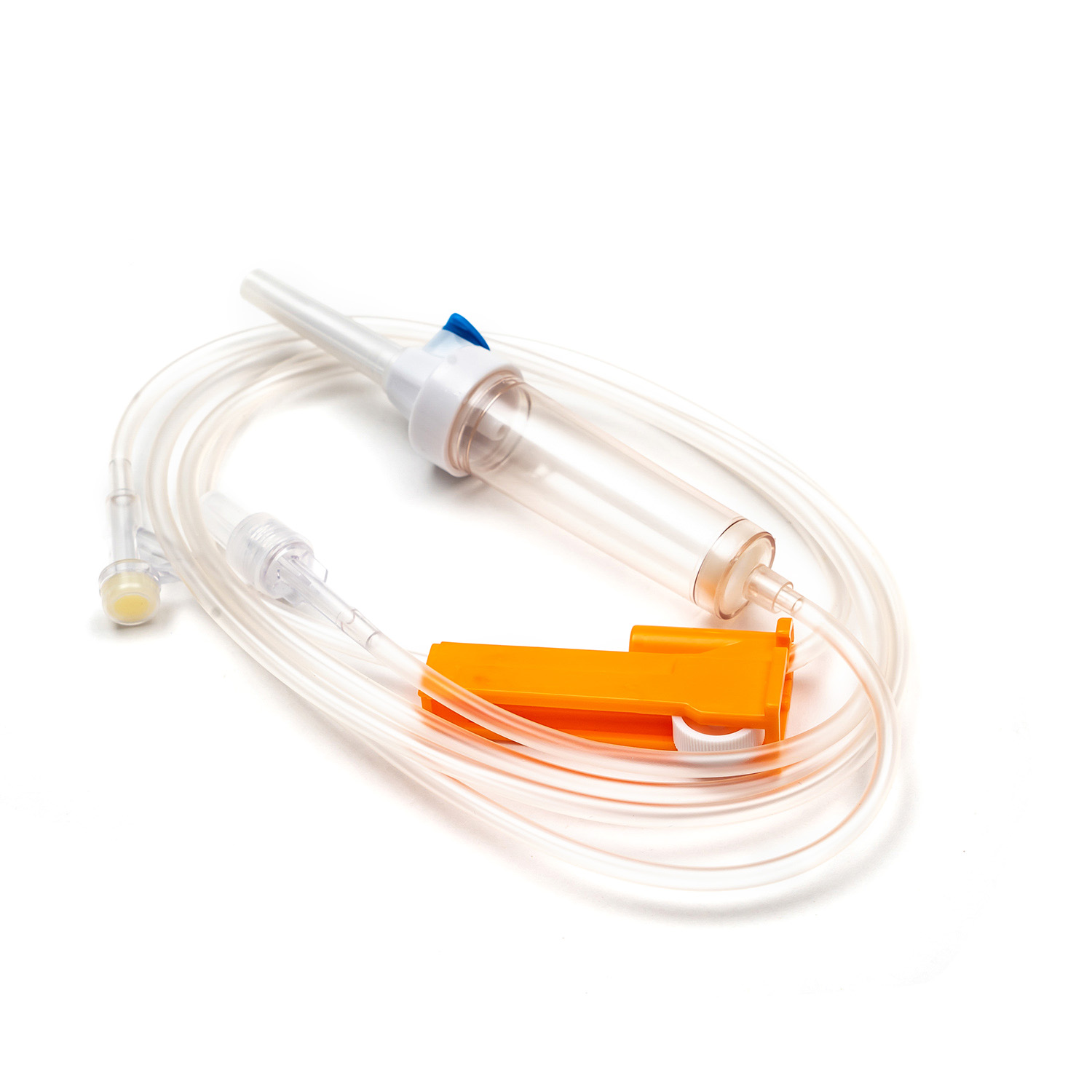
Um conjunto padrão de transfusão de sangue, embora aparentemente simples, é uma maravilha da engenharia médica projetada para precisão e segurança do paciente. Cada componente desempenha um papel vital para garantir a entrega eficaz e estéril de produtos sanguíneos.
Dispositivo de pico/piercing
O espinho , ou dispositivo de piercing, é o componente plástico rígido, nítido na parte superior do conjunto de transfusão. Sua função principal é penetrar de forma segura e assepticamente a porta da bolsa de sangue. Projetado para um ajuste confortável, evita vazamentos e mantém um sistema fechado, o que é crucial para impedir a contaminação do produto sanguíneo.
Câmara de gotejamento
Localizado logo abaixo do pico, o Câmara de gotejamento é uma lâmpada transparente e flexível. Este componente serve a vários propósitos importantes:
-
Visualização de fluxo: Ele permite que os profissionais de saúde monitorem visualmente o fluxo de sangue, observando a taxa na qual caiam, o que ajuda a calcular e manter a velocidade de infusão correta.
-
Armadilha de ar: A câmara atua como um reservatório temporário, prendendo as pequenas bolhas de ar que possam entrar na bolsa de sangue, impedindo -as de alcançar o paciente.
-
Filtro: Crucialmente, a filtro é integrado na parte inferior da câmara de gotejamento, ou logo abaixo dela. Este filtro é tipicamente um Filtro de Macropore com um tamanho de poro variando de 170 a 200 mícrons . Seu papel essencial é remover coágulos brutos, fios de fibrina ou agregados celulares que possam ter se formado no sangue armazenado. Isso impede que essas partículas entrem na circulação do paciente, onde elas poderiam potencialmente causar microemboli ou complicações pulmonares.
-
MacRodrip vs. Microdrip: O design da câmara de gotejamento também pode ditar o fator de queda, diferenciando os conjuntos de macrodrip e microdrip:
-
Conjuntos de macrodrip Forneça gotas maiores (por exemplo, 10 ou 15 gotas/ml) e são usadas para a maioria das transfusões de adultos quando é desejada uma infusão relativamente rápida.
-
Conjuntos de microdrip Produza gotas muito menores (por exemplo, 60 gotas/ml) e geralmente são reservadas para pacientes pediátricos, neonatos ou situações onde são necessárias taxas de infusão muito precisas e lentas.
-
-
Tubulação
Estender -se da câmara de gotejamento é um comprimento de tubulação flexível e transparente . Esse tubo de grau médico foi projetado para ser resistente à torção, garantindo um caminho de fluxo contínuo e desobstruído para o sangue. Sua transparência permite a inspeção visual do fluxo sanguíneo e a detecção de quaisquer bolhas ou coágulos de ar dentro da linha.
Grampo de rolo ou braçadeira de slide
Ao longo da tubulação, você encontrará um grampo de rolo ou a braçadeira deslizante . Esses mecanismos são essenciais para controlar a taxa de fluxo do sangue.
-
A grampo de rolo Permite o ajuste fino da vazão, rolando uma pequena roda ao longo da tubulação para comprimi-la gradualmente.
-
A braçadeira deslizante Oferece uma função On/Off ou um número limitado de taxas de fluxo fixo. Ambos os tipos fornecem controle imediato para iniciar, parar ou ajustar a velocidade de transfusão, conforme necessário.
Site de injeção Y/porta de acesso
Muitos conjuntos de transfusão incluem um Site de injeção em Y. or porta de acesso . Esta porta, geralmente feita de borracha auto-vedada, permite a administração intermitente ou contínua de outros fluidos compatíveis, como solução salina normal ou medicamentos, sem precisar desconectar a linha principal do paciente. Isso é particularmente útil para lavar a linha antes ou depois da transfusão.
Conector de trava Luer/conector sem agulha
Na extremidade distal da tubulação está o Conector de bloqueio de luer ou a conector sem agulha .
-
A Conector de bloqueio de luer Fornece um acessório seguro e roscado ao cateter intravenoso (iv) do paciente ou conjunto de extensão, impedindo desconexões acidentais.
-
Conectores sem agulha são cada vez mais comuns, projetados para reduzir o risco de lesões na agulha para os profissionais de saúde, mantendo um sistema fechado e estéril para se conectar ao acesso IV.
Ventilação de ar (opcional, mas comum)
Embora nem sempre esteja presente em todos os conjuntos, um ventilação de ar é uma abertura pequena, geralmente filtrada, frequentemente encontrada em conjuntos projetados para uso com recipientes rígidos (como garrafas de vidro, embora menos comuns para sangue agora) ou quando o fluxo de gravidade pode criar um vácuo. Seu objetivo é permitir que o ar entre no recipiente como saídas de fluido, impedindo que um vácuo se formasse e garantindo um fluxo de sangue contínuo e desimpedido. Para sacos de sangue flexíveis, uma ventilação de ar separada normalmente não é necessária, pois a bolsa cai como se esvazia.
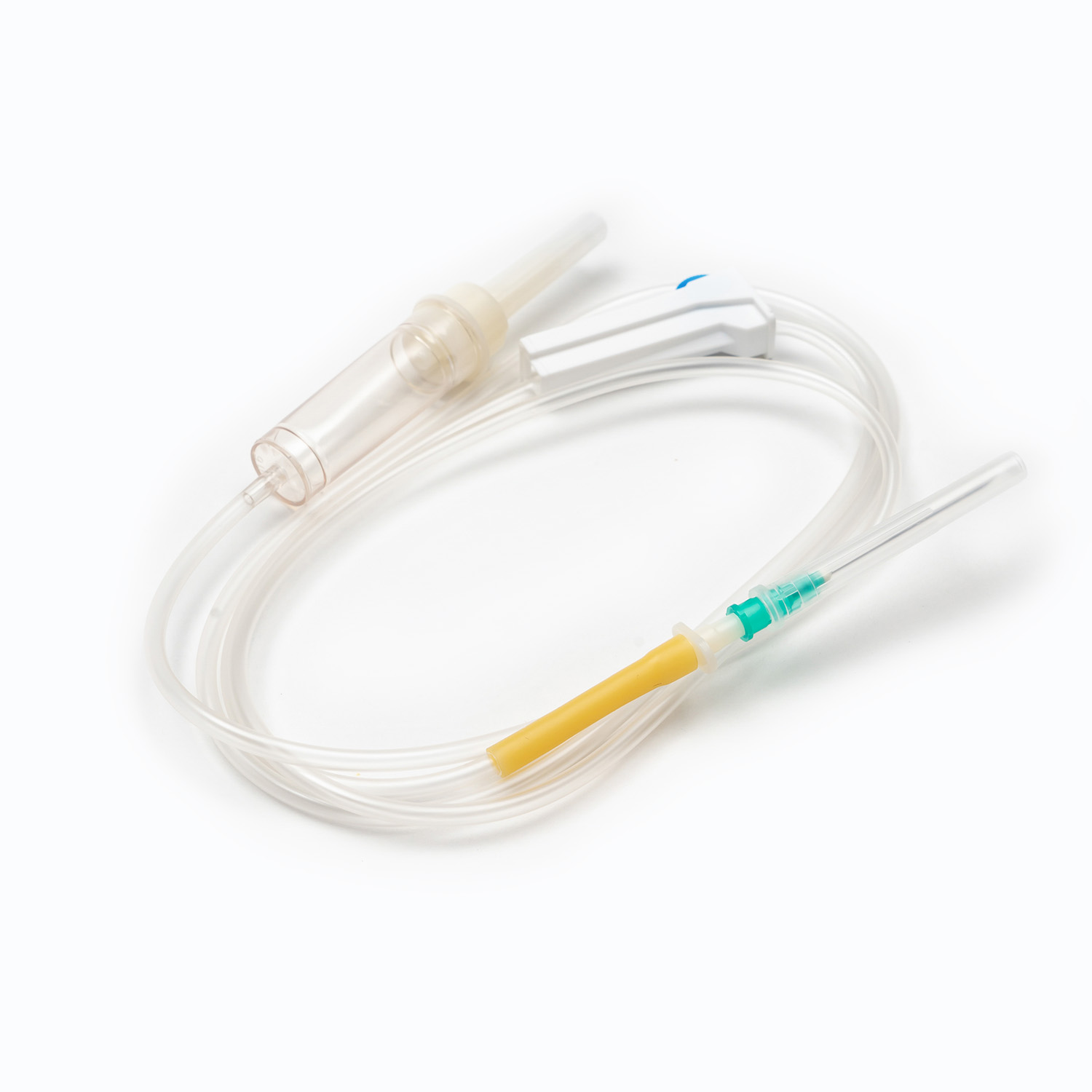
Agulha (se não um sistema sem agulha)
Se o conjunto não estiver equipado com um conector sem agulha, ele terminará em um agulha (ou uma porta para anexar uma). O medidor (Tamanho) da agulha escolhida para função venosa é crítica. Para transfusões de sangue, uma agulha de bitola maior (por exemplo, 18g ou 20g para adultos) é geralmente preferida para minimizar o estresse de cisalhamento nos glóbulos vermelhos durante a infusão, o que pode levar à hemólise e facilitar uma vazão mais rápida.
Iii. Tipos de conjuntos de transfusão de sangue (além do padrão)

Enquanto o conjunto padrão de transfusão de sangue atende à maioria das necessidades de transfusão, situações clínicas especializadas e práticas médicas em evolução levaram ao desenvolvimento de vários tipos avançados de conjuntos. Essas variações incorporam recursos ou modificações adicionais para melhorar a segurança, eficiência ou atender a populações e condições específicas de pacientes.
Conjuntos de transfusão de sangue pediátrico
Conjuntos de transfusão de sangue pediátrico são projetados especificamente para atender aos requisitos exclusivos de bebês, crianças e neonatos. A diferença mais significativa está em seus Câmara Microdrip , que oferece um volume de queda muito menor (normalmente 60 gotas/ml) em comparação com os conjuntos de macrodrip usados para adultos. Essa precisão é crucial para administrar pequenos volumes de sangue cuidadosamente titulados para evitar a sobrecarga de fluidos, um risco significativo nessa população vulnerável. Além disso, esses conjuntos geralmente apresentam Filtros primários menores ou foram projetados para serem usados com volumes menores e mais controlados, refletindo os volumes sanguíneos mais baixos e as taxas de transfusão mais lentas típicas em cuidados pediátricos.
Filtros de redução de leucócitos (filtros de leucoredução)
Filtros de redução de leucócitos , muitas vezes referido como filtros de leucoredução ou conjuntos de leucoredução, são um avanço crítico em medicina de transfusão.
-
Propósito: O objetivo principal desses filtros é Remova os glóbulos brancos (leucócitos) de produtos sanguíneos. Embora um filtro padrão remova agregados maiores, ele não remove a maioria dos leucócitos. Os leucócitos no sangue transfundido, mesmo em pequenos números, podem mediar várias reações adversas.
-
Benefícios: A remoção de leucócitos oferece benefícios clínicos significativos, incluindo:
-
Prevenção de reações de transfusão não-hemolítica febris (FNHTRS): Essas são reações de transfusão comuns causadas por citocinas liberadas por leucócitos doadores ou por anticorpos receptores que reagem a antígenos de leucócitos doadores. A leucoredução reduz significativamente sua incidência.
-
Reduzindo o risco de transmissão de citomegalovírus (CMV): O CMV é um vírus que pode residir nos leucócitos. Para pacientes imunocomprometidos (por exemplo, receptores de transplante, bebês prematuros), o sangue segura por CMV (CMV-serronegativo ou leucorizado) é crucial para evitar infecções.
-
Dimunização de aloimunização HLA: A exposição repetida a antígenos de leucócitos humanos doadores (HLAs) nos glóbulos brancos pode levar à formação de anticorpos anti-HLA no destinatário, complicando futuras transfusões e transplante de órgãos. A leucoredução minimiza esse risco.
-
Potencialmente reduzir a lesão pulmonar aguda relacionada à transfusão (trali): Enquanto o mecanismo é complexo, alguns estudos sugerem que a leucoredução pode desempenhar um papel na redução do risco de trali, uma reação de transfusão grave e potencialmente fatal.
-
-
Tipos: cabeceira vs. pré-armazenamento:
-
Leucoredução de cabeceira: Nesse método, o filtro de redução de leucócitos é integrado diretamente ao conjunto de transfusão de sangue e usado ao lado do paciente durante a transfusão. Isso era historicamente comum.
-
Leucoredução de pré-armazenamento: Este agora é o método mais prevalente e preferido. O sangue é leucordido no centro de coleta de sangue antes armazenar. Esse método é geralmente mais eficaz na remoção de leucócitos, reduz potencialmente o acúmulo de citocinas durante o armazenamento e simplifica o procedimento de cabeceira para os prestadores de serviços de saúde. A maioria dos países desenvolvidos agora possui políticas universais de leucorores de pré-armazenamento.
-
Conjuntos mais quentes do sangue
Conjuntos mais quentes do sangue são usados em conjunto com os dispositivos de aquecimento do sangue para elevar a temperatura do produto sanguíneo para quase a temperatura corporal antes da infusão.
-
Integrado ou usado em conjunto: Esses conjuntos são projetados especificamente para se encaixar em um dispositivo mais quente do sangue (geralmente apresentando um segmento de tubulação em espiral que passa pelo mais quente) ou é usado como o conjunto de transfusão padrão imediatamente a jusante de um aquecedor de sangue dedicado.
-
Propósito: O aquecimento do sangue é crítico em situações envolvendo Transfusões rápidas e massivas (por exemplo, trauma, grande cirurgia) ou para pacientes hipotérmicos . Infusão de grandes volumes de sangue frio rapidamente pode levar a hipotermia profunda no paciente, o que pode exacerbar a coagulopatia, aumentar o risco de arritmias cardíacas e prejudicar a recuperação. Os conjuntos mais quentes do sangue garantem que o sangue infundido contribua para manter a temperatura corporal central do paciente.
Conjuntos de transfusão de alto fluxo/rápido
Conjuntos de transfusão de alto fluxo ou rápido são especializados para situações que exigem entrega extremamente rápida de produtos sanguíneos, normalmente em situações de trauma, salas de operações ou protocolos de transfusão maciços .
-
Recursos de design: Esses conjuntos são caracterizados por Tubos maiores de furo e às vezes Câmaras de gotejamento maiores ou projetos de filtro simplificados (embora ainda mantenham a filtração necessária) para maximizar as taxas de fluxo. Eles são frequentemente usados com dispositivos de infusão de pressão para empurrar mecanicamente o sangue para o paciente em velocidades muito maiores do que a gravidade, poderia alcançar.
-
Aplicativo: Seu projeto prioriza a velocidade da entrega, que é fundamental quando um paciente está severamente e a restauração imediata da ressuscitação de volume e da capacidade de transporte de oxigênio são salvadores.
4. Mecanismo de ação e princípios
O ato aparentemente simples de uma transfusão de sangue depende de uma mistura de princípios físicos que o conjunto de transfusão aproveita habilmente para garantir uma entrega segura e eficaz.
Feed de gravidade
O princípio mais fundamental que rege o fluxo de sangue através de um conjunto de transfusão padrão é feed de gravidade . A bolsa de sangue é suspensa a uma altura maior que o local de acesso intravenoso do paciente (normalmente em um polo IV). Essa diferença de altura cria um gradiente de pressão hidrostático. O fluido (sangue) na bolsa, sob a influência da gravidade, exerce pressão que a força pela tubulação e na veia do paciente, que tem uma pressão mais baixa. Quanto maior a diferença de altura, maior a pressão hidrostática e, portanto, mais rápido a taxa de fluxo potencial. Esse mecanismo de fluxo passivo é simples e confiável, tornando -o uma pedra angular da administração intravenosa de líquido e sangue.
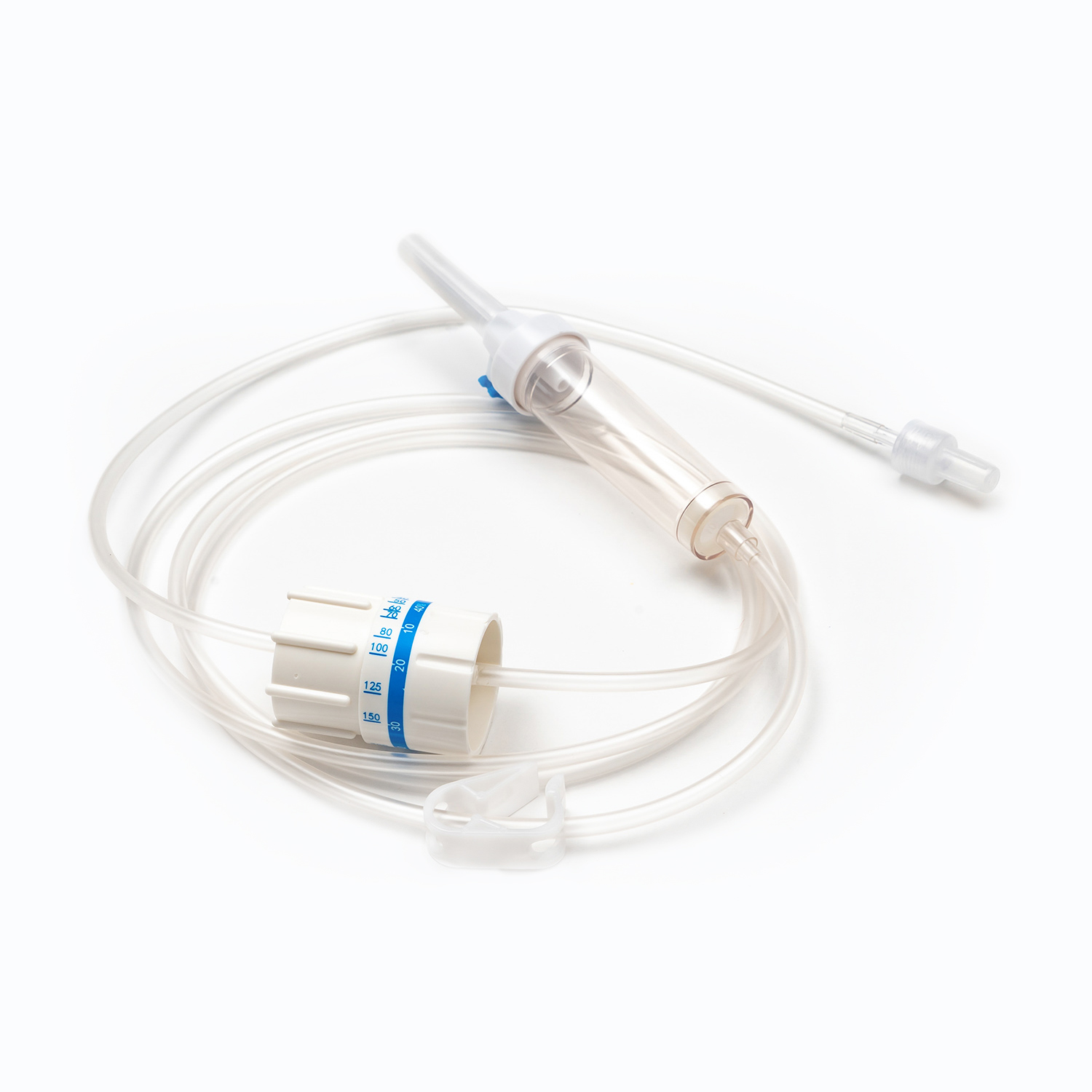
Regulação da taxa de fluxo
Enquanto a gravidade fornece a força motriz, preciso Regulação da taxa de fluxo é fundamental para garantir que o sangue seja administrado na velocidade apropriada para a condição do paciente e o tipo de produto sanguíneo. Este regulamento é alcançado principalmente através do grampo de rolo or braçadeira deslizante na tubulação.
-
Mecanismo de grampo de rolo: O grampo do rolo funciona comprimindo a tubulação flexível. Ao rolar a roda para cima ou para baixo ao longo da caixa do grampo, o usuário pode aumentar ou diminuir gradualmente a compressão na tubulação.
-
Rolando o rolo para cima (em direção à bolsa de sangue) abre progressivamente o lúmen da tubulação, diminuindo a resistência e permitindo que mais fluido flua, aumentando assim a taxa de gotejamento.
-
Rolando o rolo para baixo (Longe da bolsa de sangue) Consegue gradualmente a tubulação, aumentando a resistência e diminuindo o fluxo. Quando abaixado completamente, ocupa completamente a tubulação, interrompendo completamente o fluxo. Essa compactação precisa permite ajustes finos para atingir as quedas desejadas por minuto (GTT/min) ou mililitros por hora (ml/h), conforme prescrito.
-
Princípios de filtração
Filtração é um recurso de segurança não negociável de todos os conjuntos de transfusão de sangue. Os filtros dentro da câmara de gotejamento e filtros de redução de leucócitos especializados operam com princípios distintos:
-
Macropore (padrão) Filtração (170-200 mícrons): O filtro primário encontrado na câmara de gotejamento funciona em um exclusão mecânica princípio. Sua estrutura semelhante a uma malha com tamanhos de poros definidos (170-200 mícrons) prende fisicamente partículas maiores. Essas partículas incluem principalmente:
-
Microagregados: Pequenos grupos formados durante o armazenamento de sangue, compostos de leucócitos degeneradores, plaquetas e fibrina.
-
Fios de fibrina: Fibras de proteínas insolúveis que podem se formar no sangue armazenado.
-
Coágulos: Pequenos coágulos sanguíneos que podem ter se formado na bolsa. Ao remover esses contaminantes macroscópicos, esse filtro os impede de entrar na circulação do paciente, onde eles podem causar microemboli pulmonar, danos nos órgãos ou ativar respostas inflamatórias.
-
-
Filtração de redução de leucócitos (filtração micropore/submicron): Os filtros de redução de leucócitos (normalmente inferiores a 5 mícrons, geralmente submicron) empregam uma combinação de princípios mais sofisticada para remover glóbulos brancos, que são muito menores do que o filtro padrão pode prender:
-
Peneiração mecânica: A mídia de filtro contém poros extremamente pequenos que prendem fisicamente os leucócitos com base em seu tamanho e deformabilidade.
-
Adesão/adsorção: Este é um mecanismo crucial. O material do filtro (geralmente fibras poliméricas especialmente tratadas) possui propriedades de superfície (por exemplo, carga, hidrofilicidade) que fazem com que os leucócitos sigam as fibras do filtro à medida que o sangue passa. Glóbulos vermelhos e componentes plasmáticos, sendo menos aderentes, passam.
-
Filtração de profundidade: Em vez de apenas uma peneira plana, esses filtros geralmente têm uma matriz tridimensional tortuosa através da qual o sangue flui, aumentando a área da superfície e o tempo de contato para as células serem capturadas.
-
Esses princípios combinados garantem que o sangue entregue ao paciente não esteja apenas livre de partículas de partículas, mas, no caso de produtos leucorados, também esgotaram significativamente os glóbulos brancos, mitigando assim várias complicações relacionadas à transfusão.
V. Segurança e práticas recomendadas
Os riscos inerentes associados à transfusão sanguínea exigem protocolos de segurança rigorosos e adesão às melhores práticas, muitas das quais envolvem diretamente o uso e o manuseio adequados do próprio conjunto de transfusão de sangue. Garantir que a segurança do paciente seja fundamental e os seguintes princípios orientam a administração segura de produtos sanguíneos.
Esterilização
Todo conjunto de transfusão de sangue é fabricado e fornecido como um dispositivo estéril e de uso único . Este é um requisito não negociável. A esterilização, normalmente alcançada através de métodos como gás óxido de etileno ou irradiação gama, elimina todos os microorganismos, impedindo a introdução de bactérias, vírus ou fungos na corrente sanguínea do paciente durante a transfusão. Os prestadores de serviços de saúde devem sempre verificar a integridade da embalagem estéril antes de usar e descartar qualquer conjunto que pareça estar comprometido ou expirado.
Use único
A designação de "uso único" é crítico. Conjuntos de transfusão de sangue são projetados para Uso único em um único paciente . Reutilizar um conjunto, mesmo depois de tentar limpá-lo ou esterilizá-lo, é estritamente proibido devido à impossibilidade de garantir a esterilidade completa e o potencial de sangue ou contaminantes residuais, o que pode levar a infecções graves, contaminação cruzada ou reações adversas. Após a conclusão de uma transfusão ou se o conjunto for comprometido, ela deve ser descartada adequadamente como resíduos biológicos.
Importância do tamanho dos poros do filtro
A presença e específica tamanho de poro do filtro Dentro do conjunto de transfusão de sangue são fundamentais para a segurança do paciente. Conforme discutido, o filtro padrão de 170-200 mícrons é vital para remover coágulos e agregados maiores que se formam durante o armazenamento no sangue. Usando um conjunto sem um filtro adequado, ou um com um filtro danificado, expõe diretamente o paciente ao risco de microemboli pulmonar e outras complicações circulatórias. Para situações clínicas específicas que requerem depleção de leucócitos, os tamanhos precisos dos poros submicrônicos e as propriedades de adsorção dos filtros de redução de leucócitos são igualmente importantes para evitar reações imunologicamente mediadas e transmissão de patógenos. Sempre verifique se o tipo correto de filtro está presente para o produto sanguíneo pretendido e a necessidade do paciente.
Prevenção da embolia aérea
Um Embolia aérea - A entrada de ar na corrente sanguínea - é uma complicação potencialmente fatal de infusões intravenosas, incluindo transfusões de sangue. O design do conjunto de transfusão, juntamente com a técnica adequada, é crucial em sua prevenção.
-
Preparação adequada: Antes de conectar o conjunto ao paciente, ele deve ser meticulosamente "preparado", permitindo que o produto sanguíneo (ou solução salina, se estiver começando com uma descarga) para encher completamente a tubulação, expulsar todo o ar. Isso envolve inverter a câmara de gotejamento para preencher o filtro, apertando suavemente a câmara para enchê -la adequadamente e, em seguida, abrindo lentamente o grampo para permitir que o fluido flua por todo o comprimento da tubulação até que todas as bolhas de ar sejam expulsas da extremidade distal.
-
Conexões seguras: Garantir que todas as conexões (pico para bolsa de sangue, trava Luer no cateter IV) estejam apertadas e o seguro impede que o ar seja arrastado no sistema.
-
Monitorando a Câmara de gotejamento: A função da câmara de gotejamento como uma armadilha de ar também destaca sua importância; Deve ser monitorado regularmente durante a transfusão.
Monitoramento para reações
Embora o conjunto de transfusão seja um dispositivo de entrega, sua função adequada é parte integrante da segurança geral do processo de transfusão, que inclui Monitoramento vigilante para reações adversas . Qualquer mau funcionamento do conjunto (por exemplo, tubulação torcida, oclusão, ar na linha) pode impedir o fluxo e atrasar a observação de sinais vitais ou o início de uma reação. Os profissionais de saúde devem observar continuamente o paciente em busca de sinais de reações de transfusão (por exemplo, febre, calafrios, erupção cutânea, dispnéia, dor) durante e imediatamente após a transfusão, garantindo que o conjunto permaneça patente e funcional para permitir uma intervenção imediata se ocorrer uma reação.
Técnicas de iniciação adequadas
Como mencionado sob embolia aérea, técnicas de iniciação adequadas são fundamentais. Isso envolve:
-
Fechando todos os grampos antes de picar a bolsa de sangue.
-
Spiking da bolsa de sangue com segurança.
-
Apertando a câmara de gotejamento para preenchê -la no nível recomendado (geralmente a meio caminho).
-
Abrindo o grampo de rolo lentamente para permitir que o sangue flua através da tubulação, removendo completamente todo o ar.
-
Garantir que o filtro na câmara de gotejamento esteja totalmente imerso para evitar a captura de ar. A falha em primarem corretamente introduz o ar e pode levar a danos graves do paciente.
Compatibilidade com diferentes componentes sanguíneos
Finalmente, é essencial entender o Compatibilidade do conjunto de transfusão com diferentes componentes sanguíneos . Os conjuntos de transfusão de sangue padrão são projetados para uso com todos os principais componentes sanguíneos:
-
Células globais embaladas (PRBCs): O componente mais comumente transfundido, flui prontamente através de conjuntos padrão.
-
Plasma congelado fresco (FFP): Uma vez descongelado, o plasma transfusa bem através de conjuntos padrão.
-
Plaquetas: Enquanto as plaquetas são delicadas, os conjuntos padrão com filtros de 170-200 mícrons geralmente são adequados. Alguns produtos plaquetários podem se beneficiar de filtros de plaquetas específicos, mas isso é menos comum ao lado da cama.
-
Crioprecipitado: Este componente também flui através de conjuntos padrão.
No entanto, componentes específicos ou situações clínicas podem justificar os conjuntos especializados mencionados anteriormente (por exemplo, produtos leucorados que requerem filtros de leucoredução ou infusões rápidas que precisam de conjuntos de alto fluxo). Criticamente, Nenhum medicamento ou soluções diferentes da solução salina normal (0,9% de NaCl) devem ser infundidas através da mesma linha que o sangue, a menos que especificamente aprovado e demonstrado seja compatível , como muitos medicamentos e soluções (por exemplo, soluções de dextrose, lactato de Ringer) podem causar hemólise ou coagulação do produto sanguíneo dentro da tubulação.
Vi. Complicações relacionadas a conjuntos de transfusão (indiretamente)
Embora os conjuntos modernos de transfusão de sangue sejam projetados com segurança como prioridade, seu uso inadequado, defeitos de fabricação ou limitações inerentes podem levar indiretamente a várias complicações. Esses problemas geralmente são evitáveis através da atenção meticulosa aos detalhes e aderência aos protocolos estabelecidos.
Bloqueio/coagulação dentro do conjunto
Uma das complicações mais comuns encontradas com conjuntos de transfusão de sangue é o bloqueio ou coagulação dentro da tubulação ou filtro . Isso pode ocorrer devido a vários fatores:
-
Taxa de infusão lenta: Se o sangue for infundido muito lentamente, especialmente os glóbulos vermelhos embalados que são mais viscosos, pode gastar muito tempo na tubulação e começar a coagular.
-
Priming inadequado: Bolhas de ar residual ou lavagem insuficiente podem criar áreas onde o fluxo sanguíneo está estagnado ou turbulento, promovendo a formação de coágulos.
-
Flushing inadequado: A falha em lavar a linha com solução salina normal antes e depois de certos procedimentos (por exemplo, a administração de medicamentos através do local Y) pode levar à coagulação do sangue residual.
-
Misturando soluções incompatíveis: Infundir soluções ou medicamentos incompatíveis (por exemplo, soluções de dextrose, lactato de Ringer) através da linha sanguínea pode causar aglutinação ou hemólise dos glóbulos vermelhos, levando a coágulos que bloqueiam o filtro ou tubulação.
-
Sobrecarga de filtro: Em casos raros de produtos sanguíneos altamente coagulados ou agregados (que devem ser detectados e não transfundidos idealmente), o filtro pode ficar sobrecarregado e completamente bloqueado.
-
Tubos dobrados: As torções físicas na tubulação podem impedir o fluxo, fazendo com que o sangue estagne e coaguem proximal à obstrução.
Um conjunto bloqueado leva à interrupção do fluxo sanguíneo, atrasando as transfusões críticas e exigindo a descontinuação do conjunto e substituição atual por um novo, desperdiçando produtos sanguíneos valiosos.
Risco de infecção (se não for tratado assepicamente)
Embora o conjunto de transfusão de sangue seja fornecido estéril e projetado para uso único, há um inerente risco de infecção se não for tratado assepticamente . Enquanto o conjunto em si é estéril, a contaminação pode ocorrer durante vários estágios:
-
Embalagem comprometida: Se a embalagem estéril estiver rasgada, molhada ou danificada, a esterilidade do conjunto não poderá ser garantida e deve ser descartada.
-
Técnica asséptica inadequada: Durante a configuração, picar a bolsa de sangue, preparar a tubulação, conectar-se ao cateter IV ou acessar o site y, violações na técnica asséptica pode introduzir microorganismos. Tocar em partes estéreis do conjunto ou permitir que elas entrem em contato com superfícies não estéreis introduz diretamente patógenos.
-
Tempo prolongado de permanência: Embora não seja diretamente um problema definido, o uso prolongado de um único conjunto além das diretrizes recomendadas (por exemplo, geralmente não mais que 4 horas para sangue, ou após 2-4 unidades de PRBCs, dependendo da política da instituição) aumenta o risco de crescimento bacteriano dentro do caminho do fluido se ocorrer alguma contaminação.
-
Acesso contaminado no site Y: Empanos inadequados da porta de injeção do site Y antes de acessá-la pode introduzir a flora da pele ou bactérias ambientais na linha.
Tais violações podem levar a infecções da corrente sanguínea relacionadas ao cateter (CRBSIS) ou, mais severamente, contaminação bacteriana do próprio sangue transfundido, levando a reações de transfusão séptica, que podem ser com risco de vida.
Embolia aérea
Conforme destacado na seção de segurança, Embolia aérea continua sendo uma complicação potencial séria diretamente relacionada ao manuseio adequado do conjunto de transfusão.
-
Priming incompleto: A causa mais comum é a falha em purgar completamente todo o ar da tubulação antes de conectá -lo ao paciente. Pequenas bolhas, se não forem removidas, podem se unir em volumes maiores de ar.
-
Tubo desconectado: A desconexão acidental do conjunto de transfusão do cateter IV, enquanto a linha IV é patente e o braço do paciente é elevado pode permitir que o ar seja arrastado na veia, especialmente se houver pressão intratorácica negativa (por exemplo, durante a inspiração).
-
Bolsa de sangue vazia: Correr a bolsa de sangue completamente seco sem apertar a linha pode permitir que o ar da bolsa vazia entre na tubulação.
-
Conexões com defeito: As conexões ou rachaduras de trava Luer soltas na tubulação, embora raras, podem potencialmente permitir a entrada de ar.
A gravidade de uma embolia aérea depende do volume de ar e da velocidade de entrada. Pequenas quantidades podem ser assintomáticas, mas volumes maiores podem levar a uma falta de ar repentina, dor no peito, cianose, hipotensão e até parada cardíaca, formando uma trava de ar no ventrículo direito, obstruindo o fluxo sanguíneo pulmonar. Observação vigilante, conexões seguras e preparação meticulosa são essenciais para evitar isso.
Vii. Inovações e tendências futuras
O campo da medicina de transfusão está em evolução continuamente, impulsionada pelo desejo de aumentar a segurança do paciente, otimizar a utilização do produto sanguíneo e melhorar a eficiência. Embora o design principal dos conjuntos de transfusão de sangue permaneça amplamente consistente por décadas, inovações significativas estão surgindo e as tendências futuras apontam para sistemas cada vez mais inteligentes, integrados e centrados no paciente.
Sistemas inteligentes integrados
A tendência mais significativa é o desenvolvimento e a integração de sistemas inteligentes Isso traz automação, captura de dados e monitoramento em tempo real diretamente ao ponto de atendimento. Esses sistemas geralmente envolvem:
-
Tecnologia de código de barras e RFID: Integração de códigos de barras 2D em pulseiras de pacientes, sacos de sangue e conjuntos de transfusão, juntamente com Tags de identificação de radiofrequência (RFID) , permite verificação automatizada em vários pontos de verificação. Scanners de mão ou leitores de RFID podem confirmar "paciente certo, produto sanguíneo direito" ao lado da cama, reduzindo significativamente o erro humano na identificação do paciente e na correspondência cruzada. Isso também permite o rastreamento contínuo do produto sanguíneo, desde a doação à transfusão, aumentando a rastreabilidade da hemovigilância.
-
Verificação e documentação automatizadas: Os sistemas inteligentes podem orientar eletronicamente os médicos através de protocolos de transfusão, solicitar verificações vitais de sinais e documentar automaticamente todas as etapas do processo de transfusão. Isso reduz os erros de gráficos manuais, garante a conformidade com as políticas hospitalares e fornece um registro eletrônico abrangente para melhoria de auditoria e qualidade.
-
Monitoramento em tempo real: Conjuntos futuros podem incorporar micro-sensores que monitoram continuamente a taxa de fluxo sanguíneo, detectam bolhas de ar ou mesmo alterações sutis nas características do sangue (por exemplo, mudanças de temperatura indicando uma reação). Esses dados podem ser transmitidos sem fio aos registros eletrônicos de saúde (EHRs), alertando os prestadores de serviços de saúde sobre possíveis problemas imediatamente.
Tecnologia de filtragem melhorada
Embora os filtros de redução de leucócitos tenham sido um grande avanço, a pesquisa continua a refinar as tecnologias de filtração:
-
Redução aprimorada de leucócitos: Melhorias adicionais nos materiais de filtro e no design dos poros visam a remoção de leucócitos ainda mais eficientes e consistentes, reduzindo potencialmente os mediadores inflamatórios residuais e minimizando ainda mais os riscos de FNHTRs e outras complicações imunes mediadas.
-
Filtros de redução de patógenos: Além dos leucócitos, a pesquisa em andamento explora filtros capazes de remover ou inativar um espectro mais amplo de patógenos (bactérias, vírus, parasitas) diretamente ao lado da cama. Enquanto as tecnologias de inativação de patógenos para produtos sanguíneos são normalmente feitos antes Armazenamento em Blood Centers, uma solução robusta de filtragem de cabeceira pode oferecer uma camada adicional de segurança, especialmente para ameaças infecciosas emergentes.
-
Filtros universais: O desenvolvimento de filtros mais versáteis que podem efetivamente remover uma gama mais ampla de componentes indesejados (por exemplo, microagregados, plaquetas ativadas, certas citocinas inflamatórias), preservando a integridade e a função das células transfundidas é uma área de investigação ativa.
Recursos de segurança aprimorados
Além da integração inteligente do sistema, os aprimoramentos físicos nos conjuntos estão sendo continuamente desenvolvidos:
-
Designs anti-Kink e anti-oclusão: Novos materiais e desenhos de tubulação que são ainda mais resistentes a dobrar ou colapso, garantindo que o fluxo ininterrupto esteja sendo explorado. Alguns conceitos incluem sensores de fluxo integrados que alarme se uma oclusão for detectada.
-
Conectores avançados sem agulha: A inovação contínua em portas de acesso sem agulha se concentra em minimizar o espaço morto, prevenir a entrada bacteriana e melhorar a facilidade de uso para os profissionais de saúde.
-
Amostragem de sangue do sistema fechado: Sistemas que permitem a amostragem de sangue diretamente da linha de transfusão sem expor o sistema ao ambiente externo reduz ainda mais o risco de contaminação e o desperdício de sangue.
-
Elementos de aquecimento integrado: Embora os aquecedores de sangue separados sejam comuns, os projetos futuros podem ter elementos de aquecimento mais compactos, descartáveis ou até integrados no conjunto de transfusão, particularmente benéficos para transfusões rápidas em ambientes de emergência.
Designs mais compactos e fáceis de usar
O esforço por maior eficiência e facilidade de uso em ambientes clínicos movimentados está levando a:
-
Miniaturização: Os esforços para tornar os conjuntos de transfusão mais compactos, mais leves e fáceis de manusear, especialmente para uso em campo (por exemplo, medicina militar, serviços médicos de emergência).
-
Mecanismos de priming simplificados: Projetos que simplificam ou automatizam o processo de iniciação, reduzindo ainda mais a chance de embolia do ar e melhorando o fluxo de trabalho.
-
Aprimoramentos ergonômicos: Melhorias no design de grampos, picos e conectores para torná -los mais intuitivos e menos propensos a erros do usuário, aumentando assim a experiência geral do usuário para os prestadores de serviços de saúde.
Essas inovações destacam um futuro em que os conjuntos de transfusão de sangue não são apenas condutos, mas participantes ativos para garantir os mais altos níveis de segurança, precisão e eficiência no atendimento ao paciente.
Viii. Conclusão
O Conjunto de transfusão de sangue , muitas vezes percebido como uma peça simples de tubulação de plástico, é, na realidade, um dispositivo médico sofisticado e indispensável. Desde seu início rudimentar séculos atrás até os sistemas altamente projetados, estéreis e muitas vezes "inteligentes" de hoje, sua evolução reflete os avanços na própria medicina de transfusão.
Este dispositivo serve a um propósito singular e sustentador de vida: transferir com segurança e componentes sanguíneos com segurança e eficiência do doador para o destinatário. Todo componente, do espinho and Câmara de gotejamento com seu vital filtro , para o tubulação and grampos , é meticulosamente projetado para garantir o fluxo controlado e impedir a passagem de partículas prejudiciais e ar. Conjuntos especializados, como os para pacientes pediátricos , Redução de leucócitos , aquecimento do sangue , e Transfusões rápidas , destaque a adaptabilidade dessa tecnologia principal a diversas necessidades clínicas e requisitos de segurança rigorosos.
A inovação contínua nos conjuntos de transfusão de sangue, com tendências inclinadas para sistemas inteligentes integrados , Filtração aprimorada , e Recursos de segurança aprimorados , ressalta o compromisso contínuo com o bem-estar do paciente. Esses avanços futuros prometem uma precisão ainda maior, erro humano reduzido e uma abordagem proativa para possíveis complicações.
Por fim, o conjunto de transfusão de sangue é mais do que apenas um canal; É um elo crítico na cadeia de cuidados que salva inúmeras vidas diariamente, apoiando pacientes através de trauma, doença crônica e procedimentos médicos complexos. Seu papel, embora muitas vezes nos bastidores, permanece absolutamente fundamental para os cuidados de saúde modernos, preenchendo a lacuna entre uma doação para a vida e um paciente em necessidade.
-